Hoe werkt een accu
1.1 Energie-omzetting
Een accu, of voluit accumulator, betekent verzamelaar. Het slaat elektrische energie op om later te gebruiken. Waar een condensator alleen kleine hoeveelheden energie kan vasthouden, zet een accu energie om in chemische vorm. Bij chemische reacties komt energie vrij of wordt opgenomen, net zoals wanneer gas verbrandt. In een accu wordt deze energie niet als warmte, maar als elektriciteit vrijgegeven. deze zet chemische energie om in elektrische energie bij ontlading, en andersom bij opladen.
1.2 Chemische reacties in een accu
In een accu vinden chemische reacties plaats tussen de actieve stoffen in de elektroden (looddioxide en sponslood) en het elektrolyt (zwavelzuur). Bij ontlading wordt looddioxide gereduceerd tot loodsulfaat en sponslood geoxideerd tot loodsulfaat, waarbij elektronen worden verplaatst. Bij opladen worden deze reacties omgekeerd: loodsulfaat wordt weer omgezet in looddioxide en sponslood. Hierdoor ontstaat elektrische stroom.
1.3 Spanningsverschil
Een elektrode in verdund zwavelzuur krijgt een spanning door de vorming van loodionen. Als een andere elektrode in dezelfde elektrolyt wordt geplaatst, ontstaat er een spanningsverschil. Dit spanningsverschil, vaak aangeduid als “spanning” in volt, hangt af van de materialen van de elektroden en de concentratie van de elektrolyt.
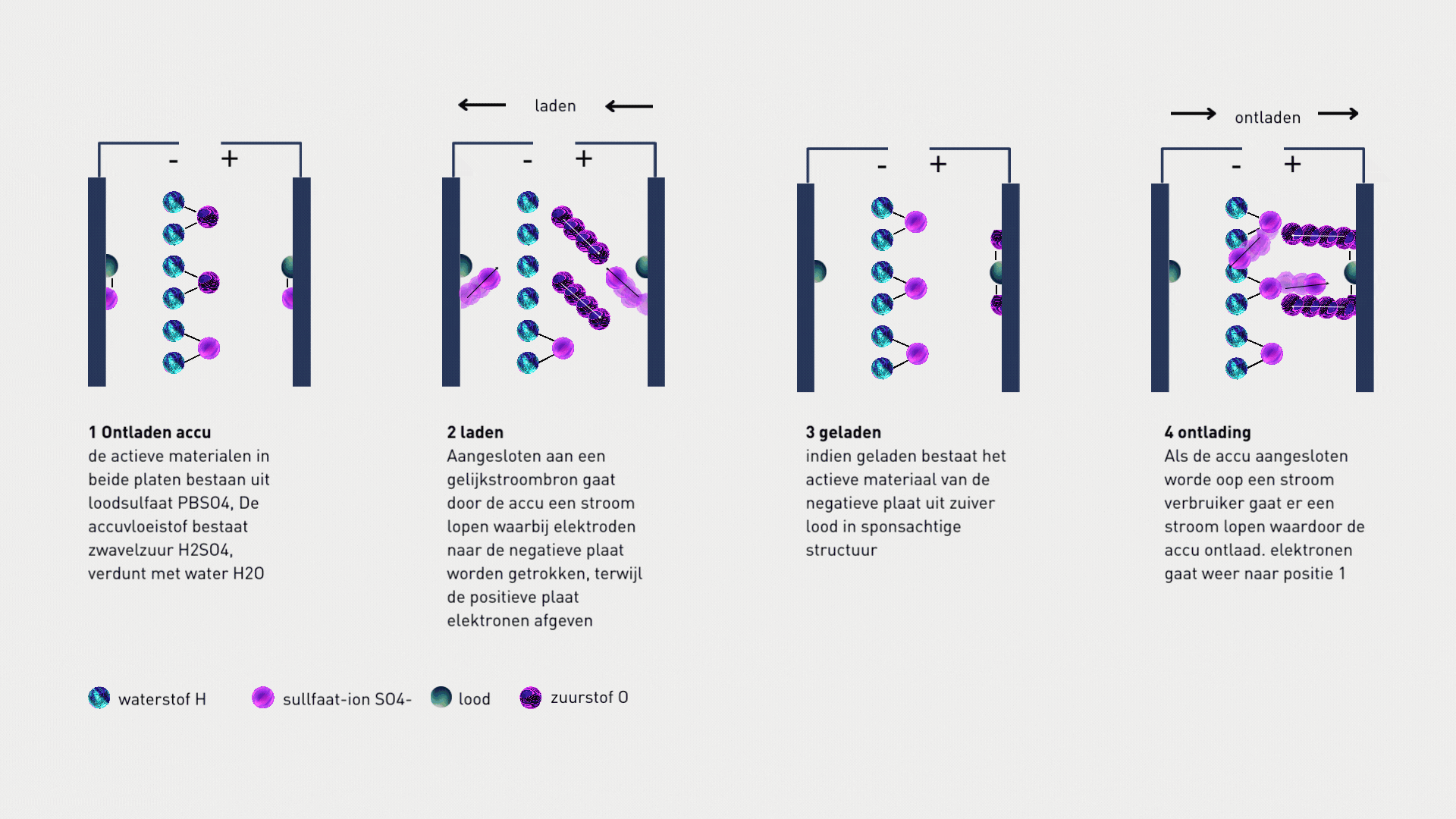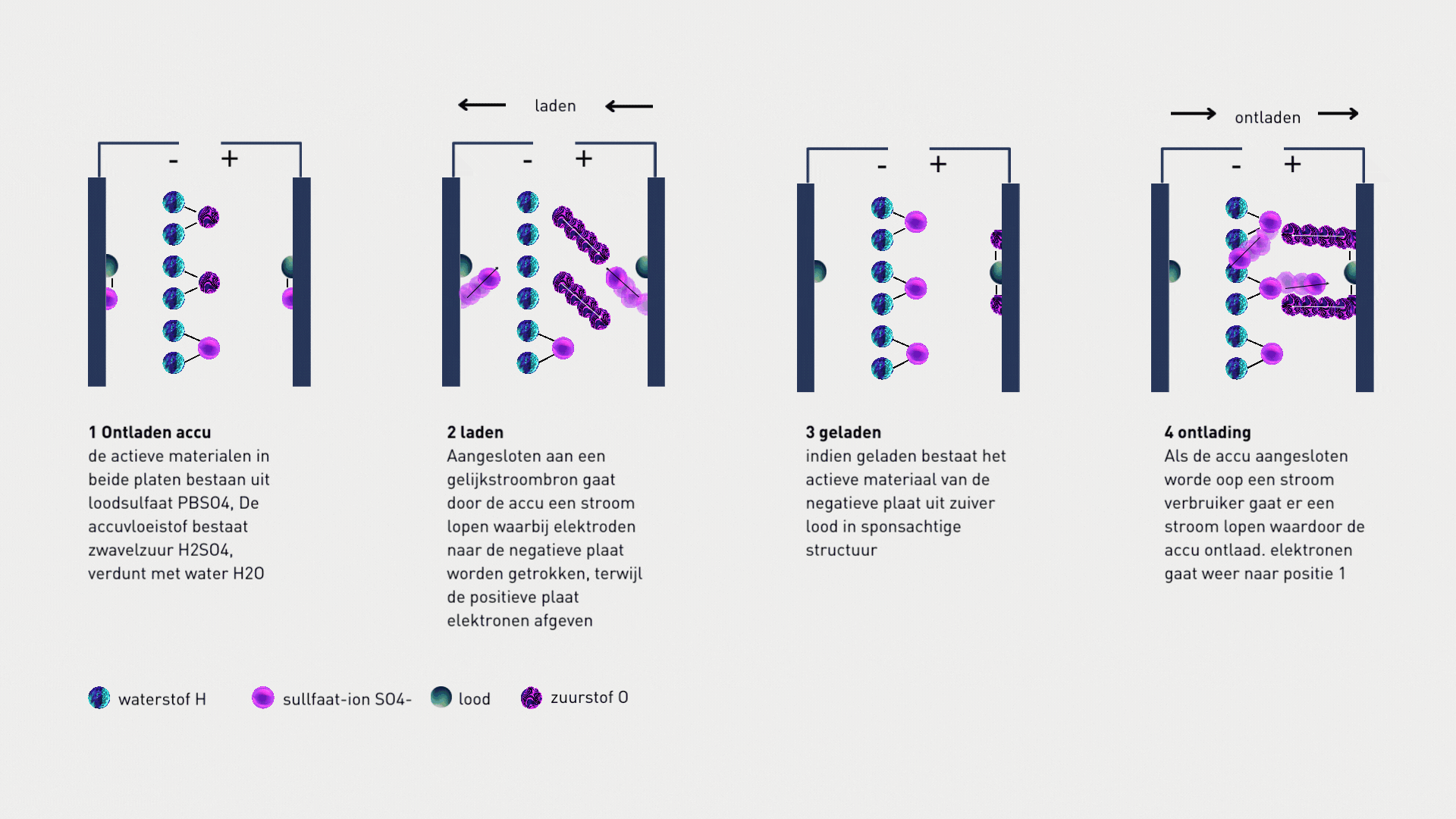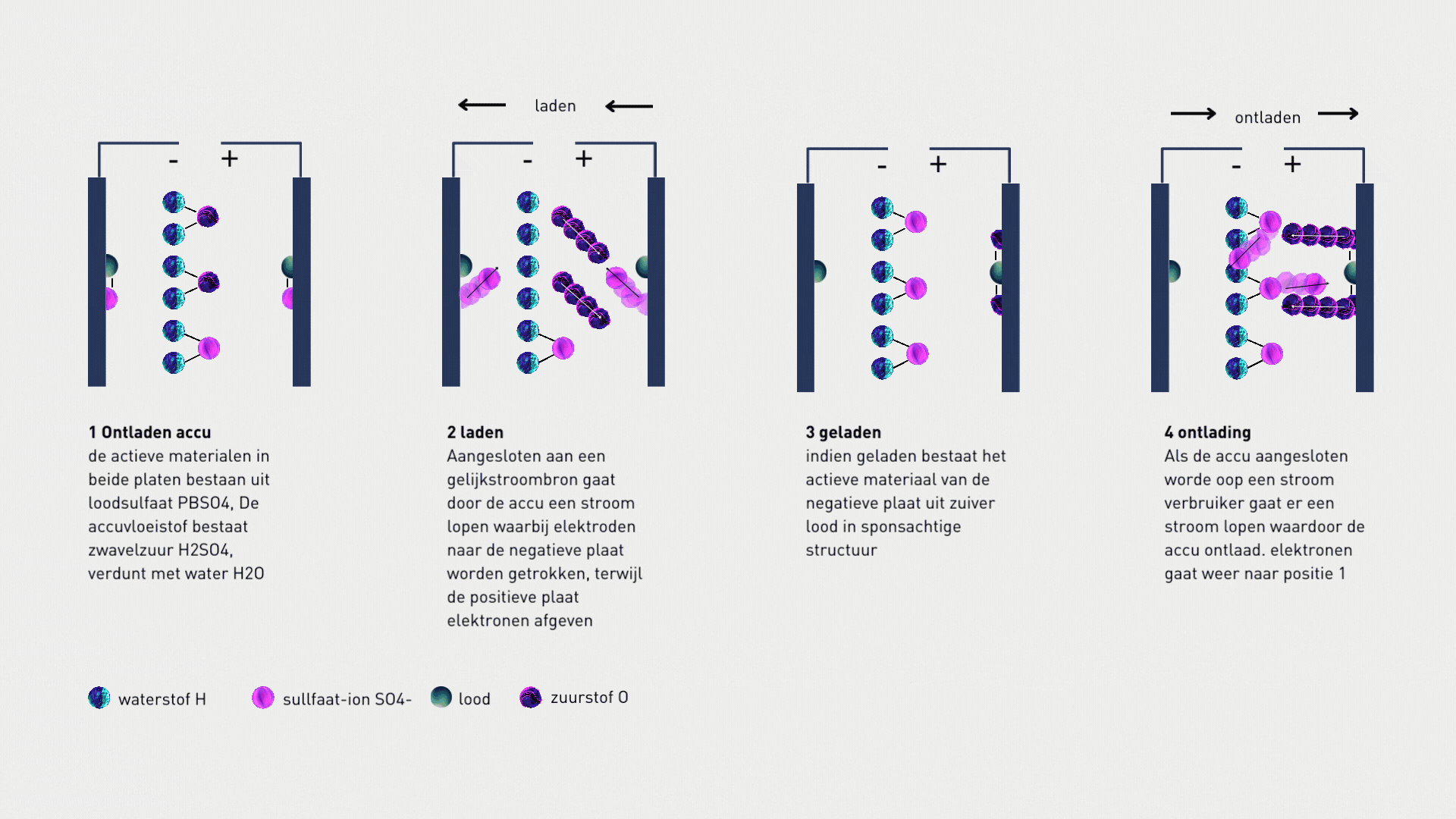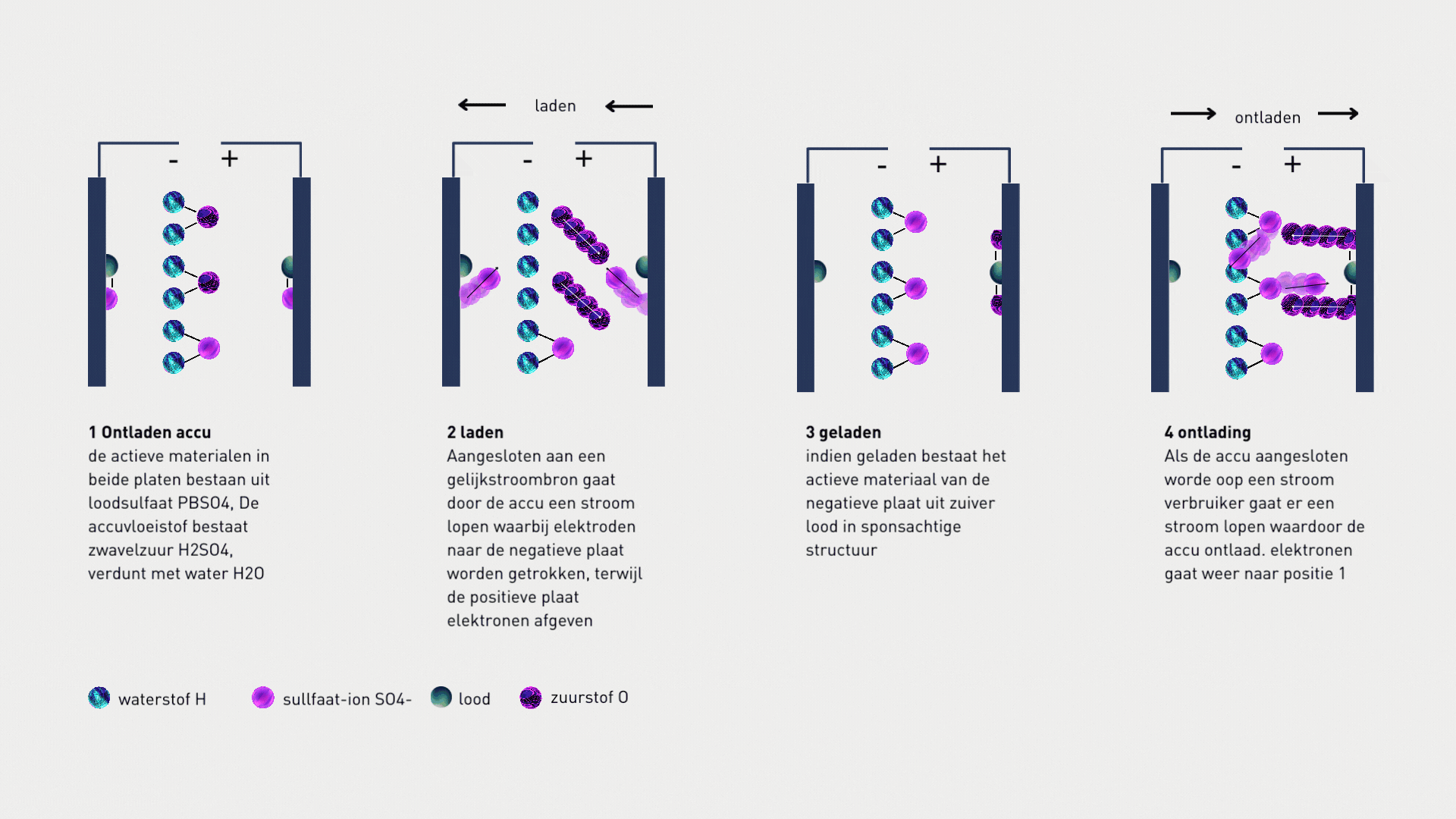
1.4 Samenvatting
Een accumulator zet elektrische energie om in chemische energie en andersom. Tijdens deze omzettingen vinden chemische reacties plaats die elektrische stroom genereren. De stroom wordt verzorgd door ionen, terwijl in de uitwendige kring elektronen stromen. Accu’s leveren gelijkstroom en de spanning is ongeveer twee volt per cel. Cellen worden in serie geschakeld om de gewenste spanning te bereiken, wat we kennen als een accubatterij of kortweg batterij.
Wil je meer weten over accu’s neem dan contact met ons op of kom nog eens vaker kijken, binnenkort een stuk over het beste onderhoud

